Investigadores del IREC consiguen desarrollar bacterias modificadas mediante biotecnología molecular que expresan proteínas de Anaplasma phagocytophilum capaces de competir con este patógeno y reducir la infección
La microbiota de las garrapatas puede ser un objetivo para el control de enfermedades transmitidas por garrapatas, como la anaplasmosis granulocítica humana (HGA, por sus siglas en inglés), causada por el patógeno Anaplasma phagocytophilum.
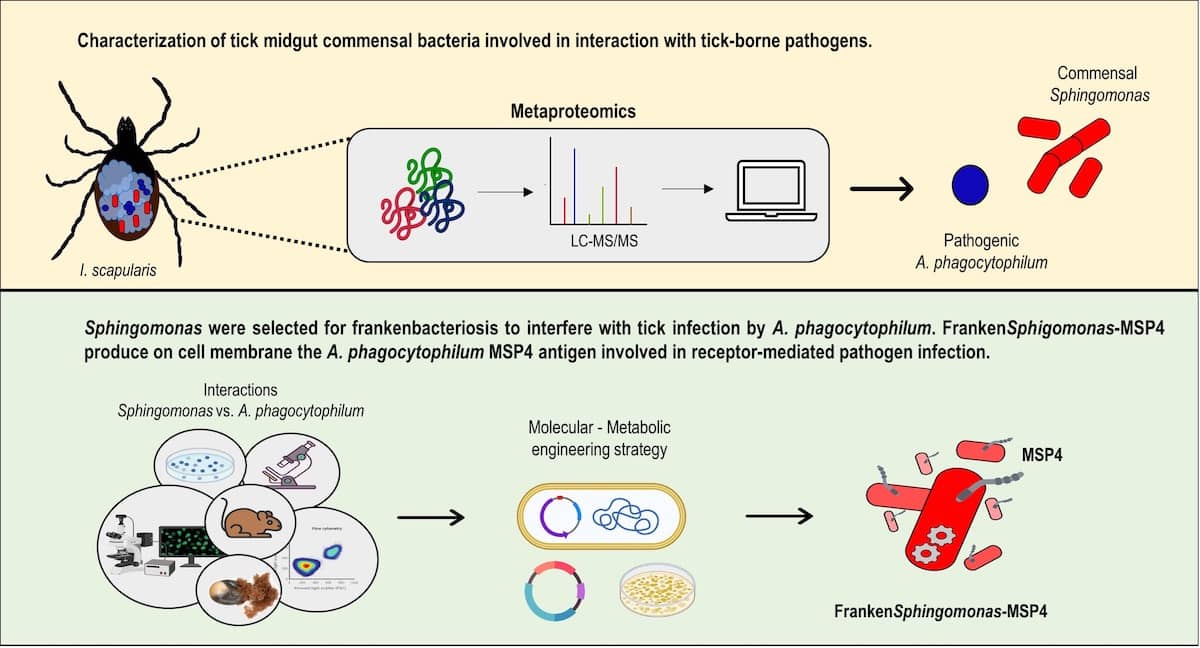
El término ”Frankenbacteriosis”, inspirado en el personaje de ficción formado por diferentes partes humanas, se ha definido en esta investigación como para-transgénesis de bacterias comensales o simbióticas de garrapatas, en este caso del género Sphingomonas, capaces de imitar y competir con los patógenos transmitidos por estos vectores. La para-transgénesis es una técnica de biología molecular que intenta eliminar un patógeno de las poblaciones de vectores mediante la transgénesis (inserción de material genético ADN de interés en un organismo receptor) de un simbionte del vector.
Mediante metaproteómica, se identificaron los géneros de bacterias de la microbiota de la garrapata que competían con el patógeno A. phagocytophilum. De esta forma, se modificaron las bacterias Sphingomonas (FrankenSphingomonas) para que produjesen la proteína MSP4 de A. phagocytophilum en su superficie.
En un primer lugar, interacciones entre el patógeno Anaplasma phagocytophilum y Sphingomonas simbióticas identificadas por metaproteómica en el intestino del vector Ixodes scapularis mostró competencias entre ambas bacterias. Por esta razón, los investigadores del Grupo de Investigación en Sanidad y Biotecnología (SaBio) del Instituto de Investigación en Recursos Cinegéticos (IREC – CSIC, UCLM, JCCM), en colaboración con científicos de otras instituciones, eligieron el género Sphingomonas como diana de para-transgénesis para el control de la infección y transmisión de Anaplasma phagocytophilum. Se eligió, entre otras candidatas, la proteína MSP4 de Anaplasma por su importante papel en las interacciones con las células hospedadores durante la infección. El material genético codificante para esta proteína fue insertado en las bacterias Sphingomonas para que estas produjesen esta proteína en su superficie.
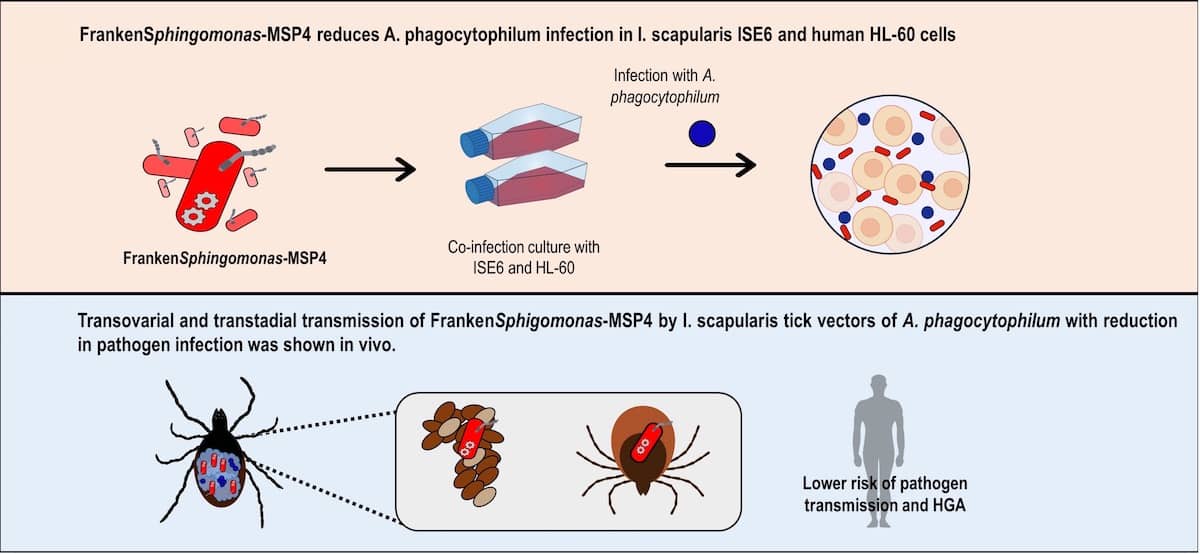
Los resultados mostraron que las bacterias FrankenSphingomonas que expresaban la proteína de superficie principal 4 (MSP4) de Anaplasma phagocytophilum (FrankenSphingomonas-MSP4) y eran co-infectadas junto al patógeno en células o roedores, imitaban la presencia del patógeno y reducían los niveles de infección en las garrapatas por competencia e interacción con los componentes del receptor celular de la infección.
La transmisión transestadial (entre estadios de vida) y transovarial (a la descendencia) de FrankenSphingomonas-MSP4 sugiere que las larvas de garrapata que contienen estas Sphingomonas genéticamente modificadas podrían ser producidas bajo condiciones de laboratorio y liberadas al exterior para competir y reemplazar las poblaciones sin modificar junto a una reducción asociada de la infección y transmisión de patógenos y riesgos de la anaplasmosis granulocítica humana.
La co-infección de FrankenSphingomonas-MSP4 y A. phagocytophilum en células de garrapata o humanas y roedores reduce la infección del patógeno in vitro e in vivo.
La metodología y protocolos llevados a cabo para realizar las modificaciones genéticas del género bacteriano Sphingomonas y expresar en ellas las proteínas de Anaplasma phagocytophilum han sido elegidos por la revista STAR protocols, de la editorial Cell Press, para ser publicados próximamente de forma individual como protocolo referente de esta técnica (https://star-protocols.cell.com/search).
Puedes consultar la publicación científica de este trabajo de investigación en:
- Mazuecos, L., Alberdi, P., Hernández-Jarguín, A., Contreras, M., Villar, M., Cabezas-Cruz, A., Simo, L., González-García, A., Díaz-Sánchez, S., Neelakanta, G., Bonnet, S. I., Fikrig, E., de la Fuente, J. 2023. Frankenbacteriosis targeting interactions between pathogen and symbiont to control infection in the tick vector. iScience 26 (5), 106697.